روزانه هزاران عمل جراحی برای جایگزینی یا ترمیم بافتهایی در اثر بیماری یا ضربه آسیب دیدهاند، انجام میشود. در حال حاضر، از انواع داربستهای مهندسی بافت، با هدف بازسازی بافتهای آسیب دیده به وسیله ترکیب سلولهای بدن با مواد زیستی به وسیله داربست بسیار متخلخل، که به عنوان الگوهایی برای بازسازی بافت عمل میکنند، جهت هدایت رشد بافت جدید استفاده میشود. این مقاله از تریتا، عملکرد و انواع مواد مورد استفاده در توسعه داربست برای انواع کاربرد داربستهای مهندسی بافت را شرح می دهد. با ما همراه باشید.
وقتی مهندسی بافت که به کمک پزشکی میآید
بیماری، صدمه و ضربه میتواند منجر به آسیب دیدن بافتهای بدن انسان شود که برای تسهیل ترمیم، جایگزینی یا بازسازی آنها به درمان نیاز است. معمولا درمان بر پیوند بافت از یک قسمت به قسمت دیگر در همان بیمار (یک پیوند خودکار) یا از فردی به فرد دیگر (پیوند یا آلوگرافت) متمرکز است. در حالی که این درمانها انقلابی و نجاتبخش بوده اند، مشکلات عمدهای در هر دو روش وجود دارد.
برداشت آلوگرافت گران و دردناک است، محدودیتهای آناتومیکی دارد و با بروز عوارض در بدن اهداکننده به دلیل عفونت و هماتوم همراه است. به طور مشابه، محدودیتهای دیگری وجود دارد. نظیر:
- آلوگرافتها و پیوندها نیز به دلیل مشکلات دسترسی به بافت کافی برای همه بیمارانی که به آنها نیاز دارند.
- خطرات رد شدن آنها توسط سیستم ایمنی بدن بیمار وجود دارد.
- احتمال ایجاد عفونت یا بیماری از فرد اهداکننده وجود دارد.
رشته مهندسی بافت با بازسازی و حفظ یا بهبود عملکرد بافت، قسمتهای آسیب دیده را به جای جایگزینی، احیا میکند.

تاریخچه مهندسی بافت
اصطلاح «مهندسی بافت» به طور رسمی در بنیاد ملی علوم در سال ۱۹۸۸ به معنی «کاربرد اصول و روشهای مهندسی و علوم زیستی در جهت درک بنیادی روابط ساختار و عملکرد در بافتهای طبیعی و پاتولوژیک پستانداران و توسعه جایگزینهای بیولوژیکی برای بازیابی، حفظ یا بهبود عملکرد بافت» به کار برده شد. با این حال، در حالی که زمینه مهندسی بافت ممکن است نسبتاً جدید باشد، ایده جایگزینی بافت با بافت دیگر به قرن شانزدهم برمیگردد. گاسپارو تگلیاکوززی (۱۵۴۶–۱۴۹۹)، پروفسور جراحی و آناتومی در دانشگاه بولونیا در کار خود با عنوان «جراحی نقص عضو با کاشت»، جایگزین بینی را که از فلپ ساعد ساخته بود، توصیف کرد.
رشته مهندسی بافت بسیار چندرشتهای است و از متخصصان پزشکی بالینی، مهندسی مکانیک، علوم مواد، ژنتیک و رشتههای مرتبط از مهندسی و علوم زیستی کمک میگیرد. این زمینه به طور گسترده به استفاده از انواع داربستهای متخلخل سهبعدی مهندسی بافت متکی است تا محیط مناسبی برای بازسازی بافتها و اندامها فراهم شود. این داربستها اساساً به عنوان الگویی برای تشکیل بافت عمل میکنند و معمولاً با سلولها و گاهی اوقات با عوامل رشد کشت میشوند، یا در معرض محرکهای بیوفیزیکی به شکل یک واکنشگر زیستی قرار میگیرند که دستگاه یا سیستمی است، که انواع مختلفی از محرکهای مکانیکی یا شیمیایی را روی سلولها اعمال میکند.
این داربستهای بذری سلول یا در شرایط آزمایشگاهی برای سنتز بافتهایی که میتوانند در محل آسیب دیده کاشته شوند، کشت میشوند یا مستقیماً در محل آسیب دیده با استفاده از سیستمهای بدن کاشته میشوند؛ جایی که بازسازی بافتها یا اندامها در داخل بدن ایجاد میشود. این ترکیب از سلولها، سیگنالها و داربست اغلب به عنوان سه گانه مهندسی بافت نامیده میشود.
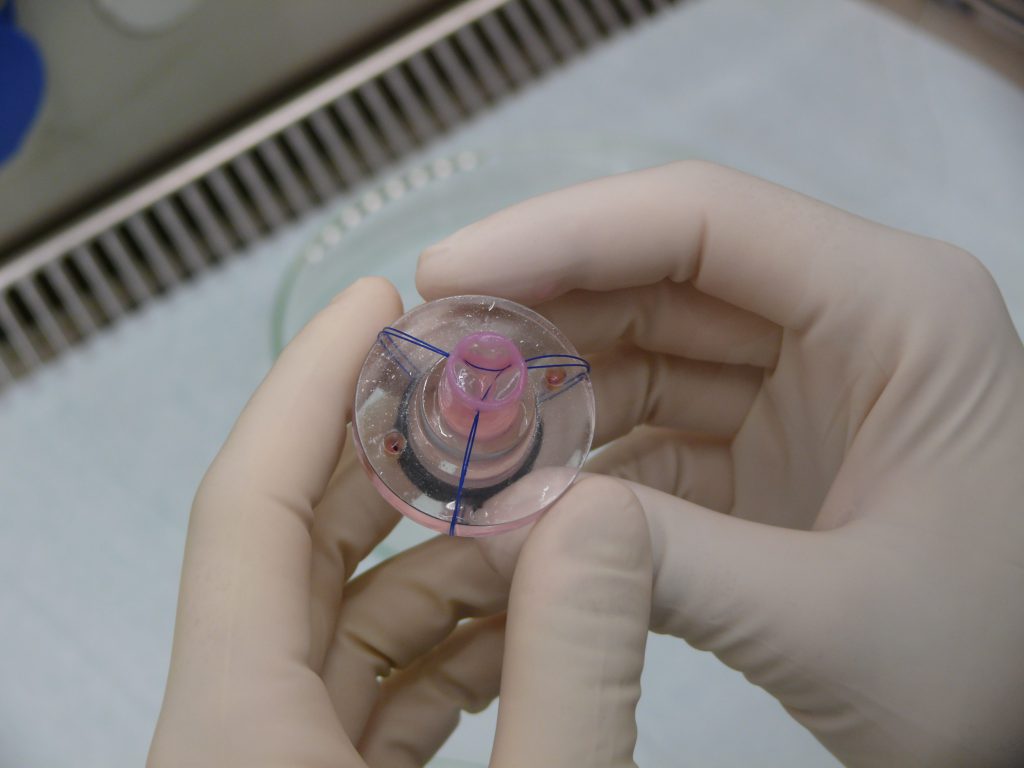
کاربرد انواع داربستهای مهندسی بافت چیست؟
چالش مهندسی بافت تقلید کردن از آن چیزی است که در طبیعت اتفاق میافتد. با این حال تلاش این حوزه، مهندسی کردن تقریباً تمام بافتها و اندامهای بدن در شرایط آزمایشگاهی است. در این حوزه، کار در زمینه ایجاد بافت کبد، عصب، کلیه، روده، پانکراس و حتی ماهیچههای قلب و دریچهها انجام میشود.
در زمینه بافتهای همبند، سالهاست که کار در زمینه مهندسی تاندون، رباط، استخوان و غضروف در سراسر جهان ادامه دارد. تا به امروز بالاترین میزان موفقیت در زمینههای پوست، مثانه، مجاری هوایی و استخوان به دست آمده است، جایی که ساختارهای مهندسی بافت، با موفقیت در بدن بیماران استفاده شده است. علاوه بر این، کاشت کندروسیت اتولوگ (ACI) و کاشت کندروسیت اتولوگ ناشی از ماتریس (MACI)، موفقیت در ترمیم غضروف را نشان میدهد. این رویکرد اخیر شامل کشت کندروسیتهای اتولوگ برداشت شده بر روی غشای مبتنی بر کلاژن به مدت چند هفته در آزمایشگاههای دارای مجوز GMP Genzyme قبل از انتقال سازه به بیمارستان، و سپس کاشت در محل آسیب دیده است. این محصول در حال حاضر برای استفاده در اروپا و استرالیا تأیید شده است.
چالشهای مهندسی بافت و انواع داربستهای آن چیست؟
در حال حاضر پیشرفتهای بزرگی در زمینه مهندسی بافت حاصل شده و فعالیتهای اقتصادی در این حوزه به طور تصاعدی در حال رشد هستند. تعداد محصولاتی که توسط این حوزه به بازار وارد میشوند در حال افزایش است و فروش سالانه بایومتریالهای احیاکننده از مرز ۲۴۰ میلیون دلار آمریکا در سال نیز عبور کرده است. با این وجود، به تحقیقات بیشتری در این زمینه احتیاج داریم.
همانطور که در بالا توضیح داده شد، فقدان عروق در داربست و سازههای مهندسی بافت یک چالش عمده است و بهبود استراتژیهای رگزایی یکی از حوزههایی است که نیازمند تحقیقات گسترده در زمینه مهندسی بافت است. یکی از راههای بهبود رگزایی، ممکن است این باشد که سلولهای موجود در داربست قبل از کاشت، ریزعروقها را مهندسی کنند.
این یک روش پیچیده است و از دیدگاه بالینی شامل برداشت اولیه سلولها از یک بیمار/ اهداکننده و سپس مهندسی کردن ریزعروق در حال رشد و به دنبال آن مهندسی کردن ماتریس/بافت مورد نظر در اطراف این عروق است؛ که همه آنها باید قبل از کاشت در بدن بیمار حاصل شوند.
بسیاری از پزشکان به دلیل نیاز به حداقل دو روش و تأخیر در درمان در حین کشت در شرایط آزمایشگاهی، تأثیر مهندسی بافت آزمایشگاهی را زیر سوال میبرند. از دیدگاه تجاری، این رویکرد همچنین به دلیل طولانی شدن فرایند نظارتی مورد نیاز قبل از تأیید چنین ساختار مهندسی بافت برای استفاده بالینی، مشکلاتی را ایجاد میکند. با این حال، در بافتهایی مانند غضروف که در صورت آسیب دیدگی توانایی بازسازی خود را ندارند، مهندسی طولانی مدت بافت در شرایط آزمایشگاهی، ممکن است تنها راه حل برای جلوگیری از نیاز به آرتروپلاستی مفصلی باشد.
بافتهای دیگر، مانند استخوان، توانایی ذاتی برای تعمیر و بازسازی را دارند. بنابراین وظیفه در زمینه مهندسی بافت، تلاش و مهار این ظرفیت احیاکننده ذاتی است. یک راه برای انجام این کار، میتواند مهندسی کردن داربست، به گونهای باشد که خود داربست سیگنالهای ترمیمی را برای سلولها فراهم کند که ممکن است نیاز به کشت طولانیمدت در شرایط آزمایشگاهی قبل از کاشت را نفی کند. بنابراین، تحقیقات زیادی در حال انجام است که به توسعه مواد زیستی پیچیدهتر با سطوح پیچیدگی بیشتر برای ترکیب چند کارکرد و داشتن بایومتریالها به داشتن ویژگیهای زیست تخمیری و پاسخگو به محرکها پرداختهاند.

نقش خواص مکانیکی سلولها در ایجاد انواع داربستهای مهندسی بافت
سلولها اطلاعات زیادی از محیط خود به دست میآورند. ماتریس بومی خارج سلولی بومی (ECM) که توسط سلولها احاطه شده و تولید میشود، از محیط اطراف خود یاد میگیرد و مجموعه فلکی پویا و ناهمگن فضایی از نشانههای ریزساختاری، ترکیبی و مکانیکی را ارائه میدهد که میتواند بر رفتار سلولها تأثیر بگذارد.
استفاده از ظرفیت مکانیکی سلولها، فرصتهای عظیمی را فراهم میکند. خواص مکانیکی بافتها، مواد بیولوژیکی، سلولها و مولکولهای زیستی دارای پیامدهای بیولوژیکی عمیقی از نظر فعالیت زیستی ایمپلنت در مقابل شکست، انتقال محرکهای مکانیکی و طیف وسیعی از فرایندها در سطح بافت، سلول و زیر سلولی است. نقشهای کلیدی در مسیرهای سیگنالینگ مولکولی توسط مجتمعهای چسبندگی سلولی و اسکلت سلولی ایفا میشود که نیروهای انقباضی آنها از طریق ساختارهای بین سلولی منتقل میشوند.
بنابراین، خواص مکانیکی بستری که سلولها به آن متصل شده اند برای تنظیم مکانیسم انتقال سلولی و رفتار سلولی بعدی بسیار مهم است. این امر پیامدهای مهمی برای توسعه، تمایز، بیماری و بازسازی دارد. برای مثال، اکنون مشخص است که سفتی بستر میتواند رفتار سلولهای بالغ و مسیر تمایز سلولهای بنیادی را تنظیم کند. به عنوان مثال، هنگامی که سلولهای بنیادی مزانشیمی روی ژلهای سفت رشد میکردند که خاصیت ارتجاعی ماهیچه را تقلید میکردند، تمایز در نسب میوژنیک (عضله ساز) مشاهده شد، در حالی که وقتی سلولهای بنیادی مزانشیمی بر روی ژلهای سفت و سختی که استخوانهای پیش کلسیفیکاسیون را تقلید میکردند رشد میکردند، سلولها از نظر استئوژنیک متمایز میشدند.
به طور مشابه، با سلولهای بنیادی عصبی، تمایز نورون بر روی داربستهای نرم که بافت طبیعی مغز را تقلید میکنند، مطلوب است، در حالی که تمایز به سلولهای گلیال حامی نورون در ماتریسهای سختتر ترویج میشود. علاوه بر این، نشان داده شده است که کاردیومیوسیتها (سلولهای ماهیچه قلب) در یک بستر با کشش شبیه قلب بهترین ضربه را میزنند، در حالی که در بسترهای سختتر، که به طور مکانیکی از زخم فیبروتیک پس از انفارکتوس تقلید میکنند، سلولها خود را بیش از حد فشار داده و ضربان را متوقف میکنند.
بنابراین، تحقیقات فزایندهای در حال استفاده از ظرفیت مکانیکی حساس سلولها برای توسعه انواع داربستهای مهندسی بافت و مواد زیستی با ویژگیهای مکانیکی خاص است که میتواند برای هدایت رفتار سلولهایی که با آنها تعامل دارند، مورد استفاده قرار گیرد.

نقش سیگنالهای بیوشیمیایی در داربستها
علاوه بر سیگنالهای بیومکانیکی، رفتار سلول به شدت تحت تأثیر سیگنالهای بیولوژیکی و بیوشیمیایی ماتریس خارج سلولی است. بنابراین، استفاده از داربستها به عنوان سیستمهای تحویل عوامل رشد، پپتیدهای چسبندگی و سایتوکاینها در این زمینه توجه قابل توجهی را به خود جلب میکند. به عنوان مثال، تلفیق عوامل رشد رگزایی در داربستها میتواند پتانسیل عروقی آنها را نیز بهبود بخشد. به طور مشابه ، روشهای تأمین عصب برای بافتهای تازه تشکیل شده نیز باید مورد توجه قرار گیرد.
یکی دیگر از حوزههای بسیار مهم، کنترل و درک پاسخ ایمنی میزبان و جلوگیری از عفونت پس از کاشت است. برای این منظور، ترکیب داروها (به عنوان مثال مهارکنندههای التهابی و/یا آنتی بیوتیکها) در داربستها به عنوان روشی برای کاهش احتمال عفونت پس از عمل جراحی پیشنهاد شده است. سرانجام ، استفاده از داربستها به عنوان سیستمهای تحویل ژنهای درمانی در حال بررسی است. بنابراین ژندرمانی میتواند ابزاری ارزشمند برای جلوگیری از محدودیتهای تحویل موضعی عوامل رشد، از جمله نیمه عمر کوتاه، نیاز به دوز زیاد، هزینه بالا، نیاز به برنامههای مکرر و توزیع ضعیف باشد.







 Optimized with PageSpeed Ninja
Optimized with PageSpeed Ninja